Polivalent sülfürün organik bileşikleri: sülfoksitler ve sülfonlar
Organik oksijen bileşikleri arasında benzerleri olmayan iki ana organosülfür bileşiği sülfoksitler ve sülfonlardır. Bu bileşiklerdeki bağ, sülfoksit için lyS (= O) ve sülfon için ―S (= O) 2 - iki kez bağlanmış yapılarla temsil edilirse, kükürt atomları sırasıyla 10 ve 12 değerlik elektronlarını “görür”. Bu, sekizli kuralının izin verdiğinden daha fazladır, ancak sülfür sekizli kuralına bağlı değildir, çünkü sülfür heksaflorür (SF 6 gibi bileşiklerde de gerekli olduğu gibi, bağlarında 3d orbitalleri kullanabilir.). Sülfür değerlik kabuğunun sekizden fazla elektron içerecek şekilde genişlemesi için bazı teorik destek olsa da, 3d orbitallerin enerji bakımından kükürt 3 ve 3p orbitallerinden çok daha yüksek olması nedeniyle 3d orbitallerin kullanımı eleştirilmiştir. Alternatif bir bağlanma modeli, sülfoksit için ―S + (―O -) - ve sülfon için ―S2 + (―O -) 2− gibi polar bağları başlatır. Polar rezonans yapılarının genel bağlanmaya katkıda bulunduğu açık olmakla birlikte, sülfür 3d orbitallerden de bir miktar katkı olması muhtemeldir. Sülfoksit grubunun, sülfür atomu üzerinde yalnız bir çift elektron içerdiği ve sülfoksit grubunun bir amine benzer, ancak bir karbonil grubunun düzlemsel yapısından (OC) oldukça farklı olması gerektiğini belirtmek gerekir.) -, bazen bir sülfoksit grubu karşılaştırılır. Sülfoksit grubunun düzlemsizliğinin önemli bir sonucu, R ve Rp'nin farklı olduğu R (S = O) R 'tipindeki sülfoksitlerin kiral oldukları ve aslında sülfon grubu ile optik olarak aktif formda izole edilebilmeleridir. tetrahedral olmak. Aminlerin aksine, fosfinlere benzer şekilde, tricoordinate sülfür (üç ligandlı trigonal piramidal sülfür bileşikleri ve sülfür üzerinde yalnız bir çift elektron - örneğin sülfinil klorürler, sülfit esterleri, sülfoksitler, tiyosülfinatlar ve sülfiliminlerde) kükürt ile daha uzun bağlar (daha az kalabalık) ve daha fazla miktarda yalnız çift s-karakteri (hibridizasyonda kullanılan toplam orbital sayısındaki s orbital yüzdesi) nedeniyle kararlı konfigürasyon. Birçok optik olarak aktif tricoordinat bileşiği doğada meydana gelir ve optik olarak aktif sülfür bileşikleri, diğer kiral bileşiklerin sentezinde yaygın olarak kullanılır.
Sülfoksitler sadece, alfabetik sıraya göre belirlenmesinden adlandırılır, -S (= O) bağlı iki organik gruplar - kelime sülfoksit ardından grubu, (örneğin, etil metil sülfoksit, CH 3 S (O) Cı- 2, H 5) veya -sülfinil- (örn. 4- (metilsülfinil) benzoik asit) partikülü kullanılarak grupların daha basit isminden bir önek oluşturulması. Sülfonların adlandırılması, sülfoksitlerin adlandırmasına benzer; partikül-sülfonil- karmaşık vakalarda kullanılır. Sülfoksitlerin çoğu renksiz sıvılar veya düşük erime noktalarına sahip katılardır. Düşük molekül ağırlıklı sülfoksit, dimetil sülfoksit (CH 3, S (= O) CH 3, DMSO), suda çözünür olan düşük toksisite sergiler ve mükemmel bir çözücüdür. Cilde hızla nüfuz etme alışılmadık bir özelliğe sahiptir ve bileşikleri cilt yoluyla bu şekilde taşıyabilir. Veteriner tıbbında, özellikle atlarda topallığın tedavisinde bir miktar kullanımı vardır. Sülfonlar genellikle renksiz kristalin katılardır. Dimetil sülfon suda çözünürdür. Diaril sülfonlar (pH 2 Carolina 6 H 4 SO 2 Cı 6 H 4, NH 2 -p; örneğin, dapson) ve ilgili bileşikler, verem, cüzzam tedavisinde kullanılmaktadır. -SO dahil Polisülfon reçineleri, 2 Cı 6 H 4 - bir polimer içinde birimi, oksitlenmeye karşı çok termal stabilite ve direnç gerektiren elektrik ve otomotiv parçaları ve diğer uygulamalar için büyük ölçekte kullanılır.
Oluşumu ve hazırlanması
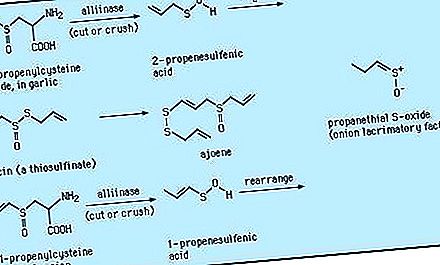
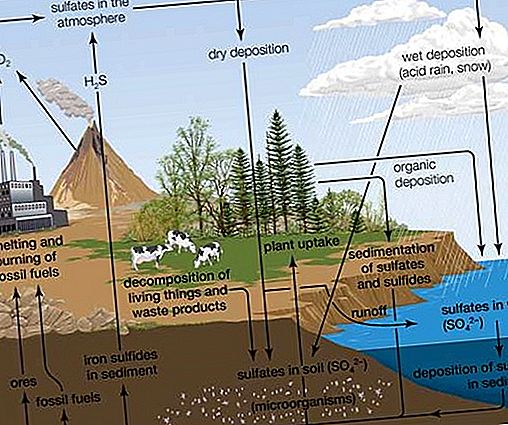
Doğal kaynaklardan izole edilen bileşikler arasında, S-alkil sistein S-oksitler (S-1- ve S-2-propenilsistein S-oksitler gibi) - Allium cinsinin bitkilerinin aroma maddelerinin öncüleri - ilk olarak karbonda ve başka bir elementte (kükürt) optik aktivite. Diğer sülfoksitlerin çeşitli yana sülforafan de dahil olmak üzere, doğal kaynaklardan izole edilmiştir (CH 3 (O) (CH 2) 4 NCS) brokoli, soğan ekstrelerinden inhibe tümör büyümesi ve zwiebelanes bildirilmiştir. DMSO, milyonda üç kısım (ppm) veya daha az seviyelerde yaygın olarak bulunur ve deniz suyu da dahil olmak üzere doğal suların ortak bir bileşenidir. Dimetil sülfon ile birlikte DMSO, alg metabolizması yoluyla üretilebilir. Yağmur suyu bulduğunda, DMSO atmosfer dimetil sülfid, (CH oksidasyonu ile sonuçlanabilir 3) 2, küresel kükürt döngüsünde biyolojik orijinli kükürt doğal transfer kısmı olarak ortaya çıkar S.
Sülfoksitler kolayca sodyum metaperiodat gibi ayıraçlarla (NAIO olan sülfidlerin oksidasyonu ile hazırlanmaktadır 4) ya da, hidrojen peroksit (H 2 O 2). Ticari olarak, DMSO dimetil sülfürün hava / nitrik oksit katalizli oksidasyonundan yapılır, bu da kâğıt üretimi için Kraft sülfat işleminin ana yan ürünüdür. Potasyum permanganat, KMnO örneğin,-gibi sülfoksitler sülfidlerin ya da daha fazlasına-kuvvetli oksitleme 4 -produces sülfonlar. Optik olarak aktif sülfoksitler, RSR ′ tipi sülfidlerin, R-R ^ 'nun, optik olarak aktif oksidanlar veya mikrobiyolojik oksidanlar ile oksitlenmesi yoluyla hazırlanabilir. Alternatif olarak, optik olarak aktif sülfoksitler optik olarak aktif sülfinil türevleri RS (= O) X, burada X = O, N veya S, R′Li veya R′MgBr gibi reaktiflerle reaksiyona sokularak hazırlanabilir. Çözücü sülfolan (tiyolan S, S-dioksit) önce sülfür (bir siklik, doymamış, beş üyeli halka sülfon) vermek üzere sülfür dioksitin bütadien ile reaksiyona sokulması, ardından sülfolan vermek üzere hidrojenleme ile hazırlanır.

Aromatik sülfonlar, sülfonil klorürlerin aromatik hidrokarbonlarla reaksiyonu yoluyla da yapılabilir. Tiyofenlerin oksidasyonu ile oluşan tiyofen S-oksitler ve S, S-dioksitler, bir veya iki çift elektronun kükürt üzerindeki oksijenle değiştirilmesinden kaynaklanan aromatiklik kaybından dolayı ana tiyofenlerden çok daha reaktiftir.













